Химия — удивительная наука. Столько невероятного можно обнаружить в, казалось бы, обычных вещах. Всё материальное, что окружают нас повсюду, существует в нескольких агрегатных состояниях: газы, жидкости и твёрдые тела. Учёные выделили ещё и 4-е — плазму. При определённой температуре какое-либо вещество может переходить из одного состояние в другое. Например, вода: при нагревании свыше 100, из жидкой формы, превращается в пар. При температуре ниже 0 переходит в следующее агрегатную структуру — лёд.
…
Весь материальный мир имеет в своём составе массу одинаковых частиц, которые между собой связаны. Эти мельчайшие элементы строго выстраиваются в пространстве и образуют так называемый пространственный каркас.
Это интересно: анионы и катионы в химии, таблица растворимости.
Определение
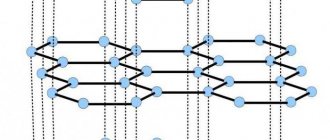
Кристаллическая решётка — особая структура твёрдого вещества, при которой частицы стоят в геометрически строгом порядке в пространстве. В ней можно обнаружить узлы — места, где расположены элементы: атомы, ионы и молекулы и межузловое пространство.
Твёрдые вещества, в зависимости от диапазона высоких и низких температур, являются кристаллическими или аморфными — они характеризуются отсутствием определённой температуры плавления. При воздействии повышенных температур они размягчаются и постепенно переходят в жидкую форму. К такого рода веществам относятся: смола, пластилин.
Это интересно: водородная связь — примеры, механизм образования.
В связи с этим можно поделить на несколько видов:
- атомную;
- ионную;
- молекулярную;
- металлическую.
Но при различных температурах одно вещество может иметь различные формы и проявлять многообразные свойства. Это явление называется аллотропной модификацией.
Это интересно: металлы и неметаллы в периодической таблице Менделеева.
МОРФОЛОГИЯ
Хорошо сформированные кристаллы встречаются редко. Кристаллы пластинчатые, чешуйчатые, изогнутые, обычно несовершенной пластинчатой формы. Чаще всего это листья без кристаллографических очертаний и их агрегаты. Образует сплошные радиально-радиальные агрегаты скрытокристаллические, листовые или округлые, реже — сферулитовые агрегаты концентрически-зонального строения. В крупнокристаллических осадках часто наблюдается треугольная штриховка на плоскостях (0001).
Ионный тип
Противоположно заряженные ионы находятся на узлах, которые создают электромагнитное поле, характеризующее физические свойства вещества. К таковым будут относиться: электропроводность, тугоплавкость, плотность и твёрдость. Поваренная соль и нитрат калия характеризуются наличием ионной кристаллической решётки.
Не пропустите: механизм образования металлической связи, конкретные примеры.
ПРОИСХОЖДЕНИЕ
Он образуется при высоких температурах в вулканических и магматических породах, пегматитах и скарнах. Он встречается в кварцевых жилах с вольфрамитом и другими минералами в среднетемпературных гидротермальных полиметаллических месторождениях. Распространен в метаморфических породах — кристаллических сланцах, гнейсах, мраморах. Крупные месторождения образуются в результате пиролиза угля под воздействием ловушек на угольных месторождениях (Тунгусский бассейн). Акцессорный минерал метеоритов. Попутные минералы: кварц, пирит, гранаты, шпинель.
Металлический тип
В своём строении напоминает молекулярную, но имеет всё же более прочные связи. Отличие данного типа в том, что на её узлах находятся положительно заряженные катионы. Электроны, которые находятся в межузловом пространстве, участвуют в образовании электрического поля. Они ещё носят название электрического газа.
Простые металлы и сплавы, характеризуются металлическим типом решётки. Для них характерно наличие металлического блеска, пластичность, тепло- и электропроводность. Они могут плавиться при различных температурах.
| Виды | Вещества | Свойства |
| Атомная | Алмаз, графит, кремний, бор | Твёрдые, тугоплавкие, не растворяются в воде |
| Молекулярная | Йод, сера, белый фосфор, органические вещества | Нетвёрдые, легко плавятся, летучие |
| Ионная | Соли, оксиды и гидроксиды тяжёлых металлов | Твёрдые, хрупкие, легкоплавкие, электропроводны |
| Металлическая | Металлы и сплавы | Блестящие, ковкие, тепло- и электропроводны. |
Свойства графита:
– электрическая проводимость графита анизотропна (т.е. зависит от направления внутри самого графита). Он хорошо проводит электрический ток в направлении, параллельном базисной плоскости. В этом случае его электропроводность близка к металлической. В перпендикулярном направлении электропроводность в сотни раз меньше.
– обладает низкой твёрдостью. Твердость школе Мооса 1.
– относительно мягкий. После воздействия высоких температур становится немного более твёрдым и очень хрупким,
– плотность 2,08-2,23 г/см³,
– легко поддается механической обработке,
– цвет от железо-черного до стально-серого, блеск металлический,
– неплавкий, устойчив при нагревании в отсутствие воздуха,
– жирный (скользкий) на ощупь, оставляет след на бумаге и пальцах,
– при трении графит расслаивается на отдельные чешуйки (это свойство используется в карандашах),
– обладает достаточно большой теплопроводностью. Теплопроводность графита анизотропна. Она составляет от 100 до 354,1 Вт/(м*К) и зависит от марки графита, от направления относительно базисных плоскостей и от температуры,
– коэффициент теплового расширения графита также анизотропен и зависит от температуры. До 700 К коэффициент теплового расширения графита отрицателен в направлении базисных плоскостей (графит сжимается при нагревании), его абсолютное значение с повышением температуры уменьшается. Выше 700 К коэффициент теплового расширения становится положительным. В направлении, перпендикулярном базисным плоскостям, коэффициент теплового расширения положителен, практически не зависит от температуры и более чем в 20 раз выше среднего абсолютного значения для базисных плоскостей,
– обладает высоким диамагнетизмом,
– химически малоактивен,
– обладает химической стойкостью. Кислотоупорен,
– при высокой температуре реагирует с кислородом, сгорая до углекислого газа,
– образует соединение включения с щелочными металлами, солями.
Различные вещества
- Алмаз. Минерал обладает высокой ценностью и после огранки используется в ювелирных украшениях. Так в чём же заключается секрет популярности этого камня? Атомы углерода составляют основу всей решётки. Между атомами минерала существует прочная ковалентная связь. Для кристаллической решётки алмаза характерно плотное содержание атомов в виде куба. Другими словами, узлами считаются атомы углерода, а своеобразными гранями куба являются прочные ковалентные связи. Такой минерал считается самым прочным на планете, и неизвестно, сколько таких своеобразных кубов включает в себя цельный алмаз.
- Графит. Углерод также может быть и в другой кристаллической модификации. Атомная решётка данного элемента включает в себя только атомы углерода, ей присуща слоистая структура. В графите каждый атом связан тремя атомами углерода. Из-за этого он обладает металлическим блеском, высокой теплопроводностью.
- Кристаллическая решётка йода имеет молекулярный тип. Атомы молекул соединяются ковалентными связями, но молекулы химического элемента имеют слабые силы притяжения. Это характеризует йод тем, что он имеет малую твёрдость, низкую температуру плавления.
- Натрий. Представитель металлической кристаллической решётки. Между катионами, расположенными в узлах решётки, двигаются электроны. Они, присоединяясь к катионам, нейтрализуют их заряд, в свою очередь, нейтральные атомы отпускают часть электронов, преобразуясь в катионы. Такой тип кристаллической решётки наделяет металл пластичностью, электро- и теплопроводностью.
- Сухой лёд. Или оксид углерода в затвердевшем виде. Имеет молекулярную кристаллическую решётку в форме куба. Молекулы удерживаются между собой слабыми связями. иффузия читайте в нашей статье.
Это интересно: как определить валентность по таблице Менделеева?
Описание графита:
Графит (в переводе с греч. – «пишу») – это природный материал, относящийся к классу самородных элементов, аллотропная модификация углерода. Химическая формула графита – C.
Наряду с графитом, алмазом существуют еще много аллотропных форм углерода. Например, графен, фуллерен, углеродные нанотрубки и т.д. Свойства данных веществ совершенно отличаются друг от друга.
Графит широко распространен в природе как минерал. Он встречается обычно в виде отдельных чешуек, пластинок и скоплений, разных по величине и содержанию.
Различают месторождения кристаллического графита, связанного с магматическими горными породами или кристаллическими сланцами, и скрытокристаллического графита, образовавшегося при метаморфизме углей.
Природный графит по своему химическому составу не отличается чистотой. В большом количестве (до 10-25%) в нем присутствует зола, состоящая из разных составляющих (Fe2O3, SiO2, Аl2O3, MgO, Р2О5, CuO, СаО и др.), газы (до 2%) и битумы, иногда вода.
Также графит получается искусственным путем различными способами. Например, нагреванием смеси кокса и пека до 2 800 °C.
Лечебное влияние
Графит обладает большим количество целебных свойств, что позволяет народной медицине активно применять его в качестве средства от болезней.
- Графит благоприятно воздействует на слои эпидермиса. Он используется при лечении кожных покровов от трещин, рубцов, синяков, экзем.
- Литотерапевты применяют графитовые изделия для лечения болезней в области носовых пазух. Камень помогает избавиться от сухости в слизистой оболочке носа, устранить различные хронические заболевания дыхательных путей, ринит, ларинготрахеит. Графит также используют в качестве профилактики лечения бронхиальной астмы.
- Камни графита способствуют улучшению состояния желудочно-кишечного тракта, налаживают процессы обмена веществ в организме, борются с хроническим гастритом, устраняют изжогу и снижают обострение запоров или диареи.
- Лечебный графит помогает справиться с сильной головной болью, апатией и стрессом.
- Графит оказывает целебное влияние на глаза человека. Маленькие камни снимают воспаление при ячмене, конъюнктивите, а также помогают в лечении катаракты или язвы роговицы.
- Минерал регулирует эмоциональный баланс, снижая уровень злости, вспыльчивости, агрессии, депрессии и неврастении.
Графит имеет кристаллическую решетку какую
В приведённой ниже таблице перечислены характерные свойства веществ с атомной и ионной кристаллическими решётками.
Характерные свойства веществ
— твёрдые при обычных условиях;
— в расплавах и растворах проводят электрический ток
| С атомной кристаллической решёткой | С ионной кристаллической решёткой |
Используя данную информацию, определите, какую кристаллическую решётку имеет:
1) хлорид кальция
;
2) графит
.
Запишите ответ в отведённом месте:
1) Хлорид кальция имеет
Хлорид кальция — вещество с ионной химической связью, тугоплавкое (Т пл = 772 °C), проводит электрический ток — имеет ионную кристаллическую решётку.
Графит — вещество с ковалентной неполярной химической связью, нелетучее, твёрдое — имеет атомную кристаллическую решётку.
Ответ: Хлорид кальция — ионная кристаллическая решётка, графит — атомная кристаллическая решётка.
Источник
Месторождения
Графитовая шахта
Востребованность графита в промышленности очень высока. На сегодня подсчитаны приблизительные запасы во всем мире в размере 600 млн тонн. Самые крупные месторождения графита находятся в Китае, Мексике, России, Чехии, Южной Корее и др. странах. Помимо перечисленных стран, графит добывают и на острове Шри-Ланка. Большие запасы этого минерала найдены и в Украине, в так называемом Завальевском месторождении. Обнаруженные выделения графита промышленно значимы и пользуются большим спросом.
Где и как добывается?
Графит добывают по всему миру. Рейтинг стран по запасам и добыче в мире представлен ниже.
- Китай. Около 780 тыс. т в год. В 2022 году страна стала крупнейшим производителем этого минерала в мире. За год Китай добыл графита столько же, сколько за предыдущие 2 года. Геологическая служба США подсчитала, что на долю этой страны приходится 65% мирового производства и 35% потребления.
- Индия. Добыто 150 тыс. тонн. Запасы месторождений варьируются от штата к штату. 43% запасов находятся в штате Аруначал-Прадеш. Всего в стране занято 8 компаний по добыче и производству графита.
- Бразилия. Добыча составляет 90 тыс. тонн в год. Все ведущие компании-производители являются частными. Уровень добычи остается прежним, но есть предпосылки вытеснения с рынка компаниями из Китая и Индии.
- Канада. Добывается 30 тыс. т графита в год. Спрос на канадский графит растет, особенно после заявления компании Тесла о закупке графита для производства батарей у компаний, сосредоточенных в Канаде.
- Мозамбик. Добыча 23 тыс. тонн. Добыча графита в этой стране выросла с нулевых отметок в 2016 году до представленной в 2022. Темпы добычи постоянно наращиваются, рынок в этом регионе представлен двумя компаниями.
Остальные страны добывают менее 20 тыс. тонн в год. Десятку стран замыкают Россия (6 место), Украина, Пакистан, Норвегия и Мадагаскар. В сумме эти страны добывают около 63 тыс. т графита в год. Рынок графита в мире постоянно растет. Связано это с переходом на электрические батареи во многих отраслях промышленности. Резкий подъем производства электромобилей по всему миру производит стимулирование спроса на графит.
Потребление в мире росло с 2013 по 2022 год, затем случилось понижение спроса на этот минерал. Цены снизились на уровень 2017 года, так как произошел переизбыток предложений и компании снизили производство для стабилизации мировых цен на минерал.
ПРИМЕНЕНИЕ
Для изготовления плавильных тиглей, футеровочных плит — применение основано на высокой термостойкости графита (в отсутствие кислорода), его химической стойкости к ряду расплавленных металлов. Он используется в электродах, в нагревательных элементах, благодаря своей высокой электропроводности и химической стойкости практически ко всем агрессивным водным растворам (намного выше, чем у драгоценных металлов). Для производства химически активных металлов электролизом расплавов, твердых смазок, комбинированных жидких и пастообразных смазок, пластиковых наполнителей.
это замедлитель нейтронов в ядерных реакторах, компонент композиции для изготовления стержней с черным графитом (в смеси с каолином). Он используется для получения синтетических алмазов в качестве эталона длины нанометрового диапазона для калибровки сканеров микроскопа с туннельным эффектом и атомно-силового микроскопа, для изготовления контактных щеток и токосъемников для различных электрических машин электромобили и мостовые краны с тележкой, мощные реостаты и другие устройства, где требуется надежный мобильный электрический контакт для изготовления тепловой защиты носовой части боеголовок баллистических ракет и возвращаемых космических кораблей.
СТРУКТУРА
Гексагональная кристаллическая полиморфная (аллотропная) модификация чистого углерода, наиболее устойчивая в условиях земной коры. Слои кристаллической решетки могут по-разному располагаться относительно друг друга, образуя целый ряд политипов, с симметрией от гексагональной сингонии (дигексагонально-дипирамидальный вид симметрии), до тригональной (дитригонально-скаленоэдрический в.с.). Кристаллическая решетка графита — слоистого типа. В слоях атомы С расположены в узлах гексагональных ячеек слоя. Каждый атом С окружен тремя соседними с расстоянием 1,42Α
Различают две модификации графита: α-графит (гексагональный P63/mmc) и β-графит (ромбоэдрический R(-3)m). Различаются упаковкой слоёв. У α-графита половина атомов каждого слоя располагается над и под центрами шестиугольника (укладка …АВАВАВА…), а у β-графита каждый четвёртый слой повторяет первый. Ромбоэдрический графит удобно представлять в гексагональных осях, чтобы показать его слоистую структуру.
β-графит в чистом виде не наблюдается, так как является метастабильной фазой. Однако, в природных графитах содержание ромбоэдрической фазы может достигать 30 %. При температуре 2500-3300 К ромбоэдрический графит полностью переходит в гексагональный.